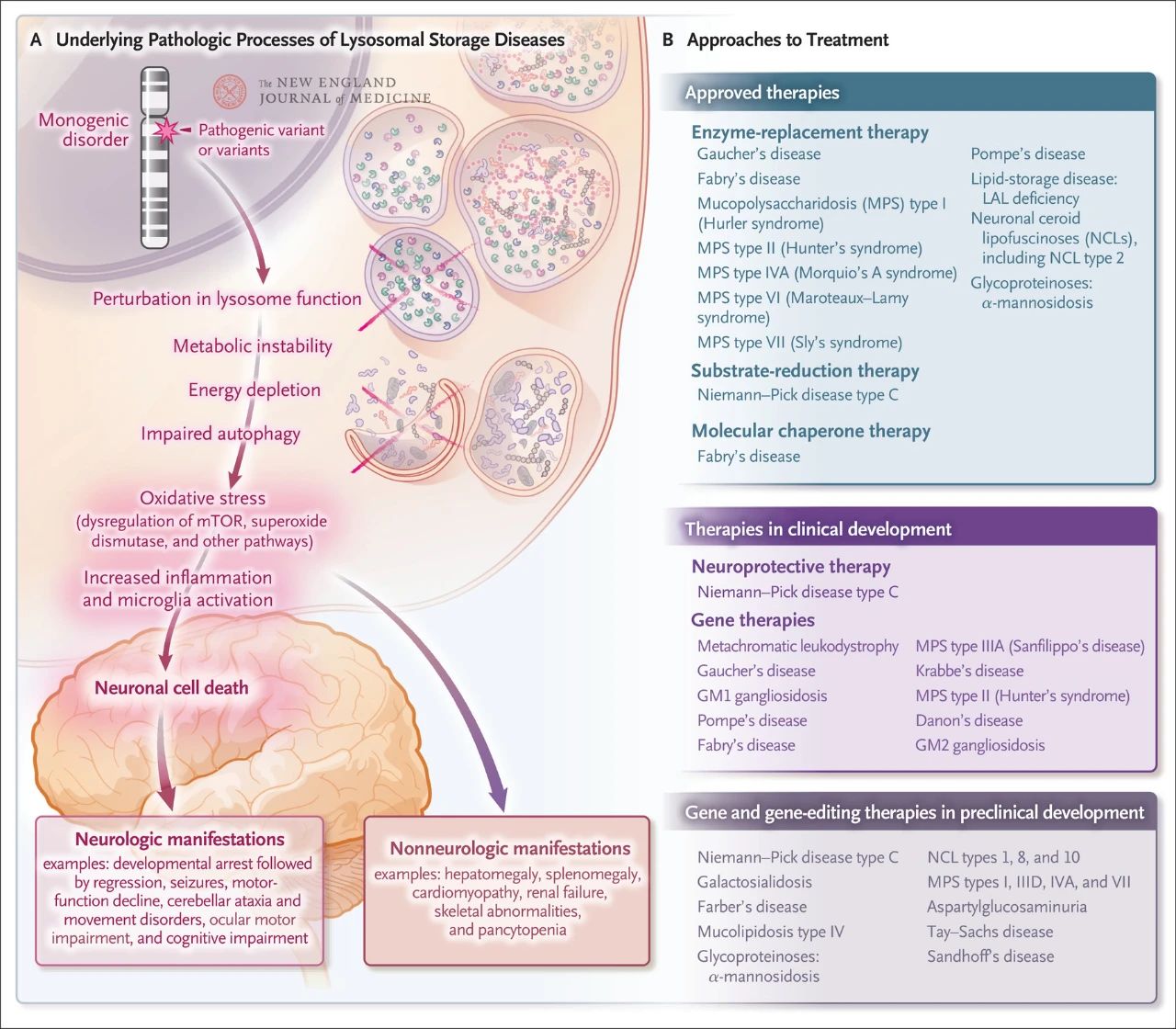
למרות היותה נדירה יחסית, השכיחות הכוללת של אגירה ליזוזומלית היא כ-1 לכל 5,000 לידות חי. בנוסף, מתוך כמעט 70 הפרעות אגירה ליזוזומליות ידועות, 70% משפיעות על מערכת העצבים המרכזית. הפרעות גן יחיד אלו גורמות לתפקוד לקוי של הליזוזום, וכתוצאה מכך לחוסר יציבות מטבולית, לחוסר ויסות של חלבון המטרה של יונקים, רפמיצין (mTOR, שבדרך כלל מעכב דלקת), לפגיעה באוטופגיה ולמוות של תאי עצב. מספר טיפולים המכוונים למנגנונים הפתולוגיים הבסיסיים של מחלת אגירה ליזוזומלית אושרו או נמצאים בפיתוח, כולל טיפול אנזימים חלופי, טיפול להפחתת סובסטרטים, טיפול מלווה מולקולרי, טיפול גנטי, עריכת גנים וטיפול נוירו-פרוטקטיבי.
מחלת נימן-פיק מסוג C היא הפרעה ליזוזומלית של אחסון כולסטרול בתאי הנגרמת על ידי מוטציות ביאלליות ב-NPC1 (95%) או ב-NPC2 (5%). התסמינים של מחלת נימן-פיק מסוג C כוללים הידרדרות נוירולוגית מהירה וקטלנית בינקות, בעוד שצורות ההתחלה המאוחרות בילדות, בילדות ובבגרות כוללות ספלנומגליה, שיתוק מבט סופרא-גרעיני ואטקסיה צרבלרית, דיסארטיקולציה ודמנציה מתקדמת.
בגיליון זה של כתב העת, Bremova-Ertl ועמיתיו מדווחים על תוצאות ניסוי כפול סמיות, מבוקר פלצבו, מוצלב. הניסוי השתמש בחומר נוירו-פרוטקטיבי פוטנציאלי, אנלוג חומצת האמינו N-acetyl-L-leucine (NALL), לטיפול במחלת נימן-פיק מסוג C. הם גייסו 60 חולים מתבגרים ומבוגרים סימפטומטיים והתוצאות הראו שיפור משמעותי בציון הכולל (נקודת הסיום העיקרית) של סולם הערכת ודירוג אטקסיה.
נראה כי הניסויים הקליניים של N-acetyl-DL-leucine (Tanganil), רצמי של NALL ו-n-acetyl-D-leucine, מונעים במידה רבה על ידי ניסיון: מנגנון הפעולה לא הובהר בבירור. N-acetyl-dl-leucine אושר לטיפול בוורטיגו חריף מאז שנות ה-50; מודלים בבעלי חיים מצביעים על כך שהתרופה פועלת על ידי איזון מחדש של קיטוב יתר ודה-קיטוב של נוירונים וסטיבולריים מדיאליים. לאחר מכן, Strupp ועמיתיו דיווחו על תוצאות מחקר קצר טווח שבו הם הבחינו בשיפורים בתסמינים ב-13 חולים עם אטקסיה ניוונית של הצרבלום מסיבות שונות, ממצאים שהציתו מחדש את העניין בבחינת התרופה שוב.
המנגנון שבו n-acetyl-DL-leucine משפר את תפקוד העצבים עדיין אינו ברור, אך הממצאים בשני מודלים של עכברים, אחד של מחלת נימן-פיק סוג C והשני של הפרעת אחסון גנגליוזיד GM2 וריאנט O (מחלת סנדהוף), מחלה ליזוזומלית ניוונית נוספת, הובילו את תשומת הלב להפנות ל-NALL. באופן ספציפי, הישרדותם של עכברי Npc1-/- שטופלו ב-n-acetyl-DL-leucine או NALL (L-אננטיומרים) השתפרה, בעוד שהישרדותם של עכברים שטופלו ב-n-acetyl-D-leucine (D-אננטיומרים) לא השתפרה, דבר המצביע על כך ש-NALL היא הצורה הפעילה של התרופה. במחקר דומה של הפרעת אחסון גנגליוזיד GM2 וריאנט O (Hexb-/-), n-acetyl-DL-leucine הביא להארכה צנועה אך משמעותית של תוחלת החיים בעכברים.
כדי לחקור את מנגנון הפעולה של n-acetyl-DL-leucine, החוקרים חקרו את מסלול המטבולי של לאוצין על ידי מדידת מטבוליטים ברקמות המוח הקטן של בעלי החיים המוטנטיים. במודל O וריאנט של הפרעת אגירת גנגליוזיד GM2, n-acetyl-DL-leucine מנרמל את חילוף החומרים של גלוקוז וגלוטמט, מגביר אוטופגיה ומגביר את רמות הסופראוקסיד דיסמוטאז (לוכד חמצן פעיל). במודל C של מחלת נימן-פיק, נצפו שינויים בחילוף החומרים של גלוקוז ונוגדי חמצון ושיפורים בחילוף החומרים של אנרגיה מיטוכונדריאלית. למרות ש-L-leucine הוא מפעיל mTOR חזק, לא היה שינוי ברמת או בזרחון של mTOR לאחר טיפול ב-n-acetyl-DL-leucine או באננטיומרים שלו באף אחד ממודלי העכברים.
ההשפעה הנוירו-פרוטקטיבית של NALL נצפתה במודל עכבר של פגיעה מוחית הנגרמת על ידי פגיעה קורטיקלית. השפעות אלו כוללות הפחתת סמנים נוירו-דלקתיים, הפחתת מוות של תאים קורטיקליים ושיפור שטף האוטופגיה. לאחר טיפול ב-NALL, התפקודים המוטוריים והקוגניטיביים של העכברים הפצועים שוחזרו וגודל הנגע הופחת.
התגובה הדלקתית של מערכת העצבים המרכזית היא הסימן המובהק של רוב הפרעות האגירה הליזוזומליות הנוירודגנרטיביות. אם ניתן להפחית את הנוירו-דלקת באמצעות טיפול ב-NALL, ניתן לשפר את התסמינים הקליניים של רבות, אם לא כולן, הפרעות האגירה הליזוזומליות הנוירודגנרטיביות. כפי שמראה מחקר זה, צפויה ל-NALL גם סינרגיה עם טיפולים אחרים למחלת אגירה ליזוזומלית.
הפרעות אגירה ליזוזומליות רבות קשורות גם לאטקסיה צרבלרית. על פי מחקר בינלאומי שכלל ילדים ומבוגרים עם הפרעות אגירה גנגליוזידיות GM2 (מחלת טיי-זקס ומחלת סנדהוף), האטקסיה פחתה והתיאום המוטורי העדין השתפר לאחר טיפול ב-NALL. עם זאת, ניסוי גדול, רב-מרכזי, כפול סמיות, אקראי, מבוקר פלצבו הראה כי n-acetyl-DL-leucine לא היה יעיל קלינית בחולים עם אטקסיה צרבלרית מעורבת (תורשתית, לא תורשתית ובלתי מוסברת). ממצא זה מצביע על כך שהיעילות עשויה להיראות רק בניסויים שכללו חולים עם אטקסיה צרבלרית תורשתית ונותחו מנגנוני הפעולה הנלווים. בנוסף, מכיוון ש-NALL מפחית נוירואינפלמציה, מה שעלול להוביל לפגיעה מוחית טראומטית, ניתן לשקול ניסויים של NALL לטיפול בפגיעה מוחית טראומטית.
זמן פרסום: 2 במרץ 2024